User:Polyethylen/Notepad2
| Polyethylen/Notepad2 |
|---|
A hepatite C é uma doença infecciosa causada pelo vírus da hepatite C (VHC) e que afecta sobretudo o fígado.[1] A infecção é muitas vezes assintomática, embora a infecção crónica possa levar à cicatrização do fígado e por fim à cirrose, que normalmente só se manifesta passado vários anos. Nalguns casos, os indivíduos com cirrose contraem Insuficiência hepática, cancro do fígado, podendo haver ainda complicações que representam risco imediato de vida, como varizes esofágicas ou gástricas.[1]
O contágio com VHC é feito através de contacto sanguíneo, associado sobretudo ao uso de seringas, material médico mal esterilizado e transfusões sanguíneas. Estima-se que em todo o mundo sejam afectadas pela hepatite C 130 a 170 milhões de pessoas. A existência da hepatite C foi proposta durante a década de 1970 e demonstrada em 1989.[2] A doença afecta apenas o ser humano e os chimpanzés.[3]
O vírus permanece no fígado em cerca de 85% dos casos de infecção. Esta infecção crónica pode ser tratada com medicação: a terapia convencional consiste numa combinação de peginterferona e ribavirina, os quais podem ser complementados com boceprevir ou telaprevir em determinados casos. A taxa de sucesso do tratamento situa-se entre os 50 e 80%. Os indivíduos que desenvolvam cirrose ou cancro do fígado podem vir a necessitar de um transplante de fígado. A hepatite C é a principal causa de transplantes de fígado, embora o vírus normalmente se volte a manifestar mesmo depois do transplante.[4] Não existe ainda uma vacina eficaz contra a doença.
Sinais e sintomas[edit]
Infecção aguda[edit]
A infecção da hepatite C manifesta-se através de sintomas agudos em 15% dos casos.[5] Os sintomas são geralmente pouco intensos e imprecisos, incluindo a falta de apetite, fadiga, náuseas, dores musculares ou nas articulações e perda de peso.[6] A maior parte dos casos de infecção aguda não tem relação com a icterícia.[7] A infecção desaparece por si própria e de forma espontânea em 10 a 50% dos casos, o que ocorre com mais frequência em indivíduos jovens do sexo feminino.[7]
Infecção crónica[edit]
Cerca de 80% daqueles que são expostos ao vírus contraem uma infecção crónica.[8] Durante as primeiras décadas, a maior parte dos infectados não nota qualquer sintoma significativo,[9] embora a hepatite C crónica esteja associada à fadiga.[10] Após vários anos, a doença torna-se a principal causa de cirrose e de cancro do fígado.[4] Cerca de 10 a 30% dos indivíduos infectados desenvolve cirrose num prazo de 30 anos.[4][6] A cirrose é mais frequente entre os que estão igualmente infectados com a hepatite B ou o VIH, entre alcoólicos e em indivíduos do sexo masculino.[6] Os que desenvolvem cirrose apresentam um risco vinte vezes maior de contrair um hepatocarcinoma, ao ritmo de 1 a 3% ao ano,[4][6] e no caso de estar associado ao excesso de álcool o risco aumenta para 100 vezes.[11] A hepatite C está na origem de 27% dos casos de cirrose e de 25% dos casos de hepatocarcinoma em todo o mundo.[12]
A cirrose hepática pode levar à hipertensão portal, acumulação de líquidos no abdómen, susceptibilidade a hemorragias, varizes (sobretudo no estômago e esófago], icterícia, e um síndroma de alteração psíquica conhecido como encefalopatia hepática. É uma das causas mais comuns na requisição de transplantes hepáticos.[13]
Extrahepáticos[edit]
Ainda que muito raramente, a hepatite C raramente está associada ao Síndrome de Sjögren (um transtorno auto-imune), à trombocitopenia, ao lichen planus, à diabetes mellitus e a transtornos linfoproliferativos das células B.[14] Estima-se que a trombocitopenia se manifeste eentre 0,16% a 45,4% dos indivíduos com hepatite C crónica.[15] Têm também sido apontadas associações prováveis com o prurigo nodularis[16] e com a glomerulonefrite membranoproliferativa.[10] A infecção por hepatite C está ainda associada a uma condição conhecida como crioglobulinemia, uma inflamação dos vasos sanguíneos pequenos e médios causada pela deposição de complexos imunes envolvendo crioglobulinas.[17]
Virologia[edit]
O vírus da hepatite C (VHC) é um Vírus ARN de senso positivo, de reduzida dimensão, de estirpe única e encapsulado.[4] É um membro do género hepacivírus da família Flaviviridae.[10] Existem sete principais genótipos de VHC, ordenados de um a sete.[18] Nos Estados Unidos, cerca de 70% dos casos têm origem no genótipo 1, 20% no genótipo 2, sendo atribuído a cada genótipo restante cerca de 1% dos casos.[6] O genótipo 1 é igualmente o mais comum na América do Sul e na Europa.[4]
Contágio[edit]
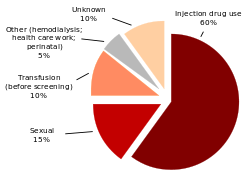
A principal forma de contágio em países desenvolvidos é através da partilha de seringas, enquanto que nos países em desenvolvimento o contágio tem origem sobretudo em transfusões sanguíneas e práticas clínicas pouco seguras.[19] A causa do contágio é desconhecida em cerca de 20% dos casos,[20] embora se acredite que possam ser contabilizados na partilha de seringas.[7]
Partilha de seringas[edit]
A partilha de seringas é um dos maiores comportamentos de risco para a transmissão da hepatite C em grande parte do mundo.[21] Entre 77 países que dispõem de dados, 25 deles revelaram ter taxas de prevalência de hepatite C entre a população de toxicodependentes de 60% a 80%,[8][21] e doze deles superior a 80%.[8] Acredita-se que dez milhões de toxicodependentes estejam infectados com a doença. A China (1,6 milhões), Estados Unidos (1,5 milhões) e a Rússia (1,3 milhões) são os países com o maior número absoluto de infecções.[8] A incidência de hepatite C entre reclusos nos Estados Unidos, por exemplo, é dez a vinte vezes maior do que a verificada na generalidade da população. Tem sido apontada como causa a existência de múltiplos comportamentos de alto risco dentro das prisões como a troca de seringas durante o consumo de drogas e a tatuagem com equipamento não esterelizado.[22][23]
Contágio em meio hospitalar[edit]
As transfusões sanguíneas, as transfusões de produtos sanguíneos, ou o transplante de órgãos sem o devido rastreio do vírus da hepatite C representam um avultado risco de infecção.[6] O rastreio universal de VHC tornou-se obrigatório no Canadá em 1990[24] e nos Estados Unidos em 1992.[25] Esta medida reduziu o risco de contágio de uma em cada 200 unidades de sangue[25] para entre uma em cada 10.000 a 10.000.000 unidades de sangue.[7][20] Embora muito residual, o risco de contágio continua a existir, já que entre o momento em que um potencial dador de sangue é infectado e a possível detecção da doença através de análises tem que decorrer um período de 10 a 70 dias, dependendo do método usado.[20] Devido ao elevado custo financeiro dos testes, alguns países ainda não rastreiam a presença de hepatite C.[12]
Indivíduos que tenham sido alvo de uma lesão provocada por uma agulha contaminada com VHC têm uma probabilidade de 1,8% de vir a contrair a doença.[6] O risco é maior se a agulha em questão é oca ou o golpe é profundo.[12] Embora baixo, existe também algum risco na exposição de mucosas ao sangue infectado, não havendo no entanto qualquer risco se a exposição ao sangue infectado ocorrer na pele intacta.[12]
O equipamento hospitalar tem igualmente sido referido como um dos meios de transmissão da hepatite C, através da reutilização de seringas, da reutilização de recipientes para administração de medicamentos, de sacos de infusão, e de equipamento cirúrgico mal esterilizado, entre outros factores de risco.[12] A ausência ou insuficiente implantação de medidas estritas de prevenção em instalações clínicas ou dentárias, públicas ou privadas, é apontada como a principal causa da disseminação do VHC no Egipto, o país com a maior taxa de infecção em todo o mundo.[26]
Relações sexuais[edit]
A probabilidade da transmissão da hepatite C através de contacto sexual é uma questão controversa.[27] Embora haja uma associação entre comportamentos sexuais de risco e a hepatite C, desconhece-se se a transmissão da doença se deve à própria actividade sexual enquanto factor de risco ou ao consumo não admitido de drogas.[6] A maioria das conclusões sustenta que não haja risco para casais heterossexuais monogâmicos.[27] No entanto, são factores de risco as práticas sexuais que envolvam um maior risco de trauma da mucosa anogenital, como o sexo penetrativo anal, ou práticas que sejam realizadas quando haja uma doença sexualmente transmissível concorrente, como o VIH ou úlceras genitais.[27] Nos Estados Unidos, o uso de preservativo enquanto método de protecção contra a hepatite C, é apenas recomendado no contexto de múltiplos parceiros sexuais.[28]
Piercings e tatuagens[edit]
Uma tatuagem representa um risco duas a três vezes maior de contrair hepatite C.[29] Isto pode dever-se tanto à má esterilização do equipamento como à própria contaminação da tinta usada.[29] As tatuagens ou piercings realizados antes de meados da década de 80, de forma clandestina ou de forma não profissional são um motivo de preocupação adicional, uma vez que é provável que não tenham sido usados quaisquer mecanismos de esterilização. O risco também aparenta ser maior consoante a dimensão da própria tatuagem.[29] Estima-se que cerca de metade dos reclusos partilhem equipamento de tatuagem não esterilizado.[29] It is rare for tattoos in a licensed facility to be directly associated with HCV infection.[30]
Partilha de objectos de uso pessoal[edit]
Determinados objectos de uso pessoal, como lâminas de barbear, escovas de dentes ou material de manicura e pedicura, podem estar contaminados com sangue. A partilha destes objectos pode eventualmente levar à exposição ao VHC.[31][32] Deve haver cuidados redobrados na presença de qualquer estado clínico que envolva hemorragias, como feridas e cortes.[32] O VHC não se transmite através do simples contacto físico, como um abraço, beijo ou partilha de utensílios de cozinha ou de refeição.[32]
Transmissão vertical[edit]
A transmissão vertical da hepatite C de uma mãe infectada para o filho ocorre apenas em menos de 10% das gravidezes.[33] Não há medidas que possam diminuir o risco.[33] Não é ainda claro o momento em que durante a gravidez se dá o contágio, mas pensa-se que possa ocorrer entre a gestação e o parto.[20] Os trabalhos de parto longos estão associados a um maior risco de transmissão.[12] Não há ainda provas de que a amamentação transmita o VHC embora, como medida preventiva, a mãe portadora da doença seja aconselhada a evitar amamentar caso os mamilos se apresentem gretados, haja hemorragias locais,[34] ou se se verifique que os níveis virais estão altos.[20]
Diagnóstico[edit]

Estão disponíveis vários testes de diagnóstico de hepatite C, entre eles a detecção do anticorpo do VHC através do ELISA, o Western blot, e a análise quantitativa da reacção em cadeia da polimerase (RCP) do ARN do VHC.[6] O ARN do vírus consegue ser detectado pela RCP normalmente entre uma a duas semanas depois da infecção, enquanto que métodos com base na detecção de anticorpos só possam ser feitos passado muito mais tempo, uma vez que os anticorpos demoram comparativamente muito mais tempo a ser formados.[13]
Define-se como hepatite C crónica qualquer infecção em que o VHC persista por mais de seis meses, tendo como base a presença ou não do seu ARN.[9] As infecções crónicas são geralmenet assintomáticas durante as primeiras décadas,[9] e descobertas frequentemente através da investigação de altos níveis de enzimas hepáticas ou durante exames de rotina em grupos de alto risco. Os exames não conseguem distinguir entre infecções agudas ou crónicas.[12]
Serologia[edit]
A detecção de Hepatite C tem normalmente início com um exame sanguíneo que detecte a presença de anticorpos do VHC, recorrendo-se a um imunoensaio enzimático.[6] Caso o resultado seja positivo, é realizado um novo teste que confirme o imunoensaio e que determine a carga viral. A verificação do imunoensaio anterior é feita com recurso a um ensaio de imunoblot recombinante, e determina-se a carga viral através da reacção em cadeia da polimerase do ARN do VHC.[6] Caso não se detecte o ARN do vírus mas o imunoblot seja positivo, significa que a pessoa já teve anteriormente uma infecção que entretanto desapareceu, quer de forma espontânea quer com recurso a tratamento. Caso o imunoblot seja igualmente negativo, significa que o primeiro imunoensaio estava errado e se tratou de um falso positivo.[6] É preciso entre seis e oito semanas a partir da data de infecção para que o imunoensaio possa apresentar resultados positivos.[10]
Os níveis de enzimas durante a fase inicial da infecção variam bastante[9] e, em média, só começam a subir sete semanas depois da infecção.[10] O nível de enzimas hepáticas pouca relação tem com a intensidade da doença.[10]
Biópsia[edit]
Para determinar o grau de danos ao fígado recorre-se a biópsias hepáticas; existem, no entanto, riscos associados ao procedimento.[4] As alterações normalmente observadas são linfócitos dentro do parênquima, gânglios linfáticos na tríade portal e alterações nos canais biliares.[4] Estão disponíveis uma série de exames sanguíneos para tentar determinar o grau de fibrose hepática e diminuir a necessidade da realização de uma biópsia.[4]
Rastreio[edit]
Acredita-se que apenas 5% a 50% dos indivíduos infectados nos Estados Unidos e Canadá estão conscientes de que estão infectados.[29] O rastreio é recomendado em grupos de alto risco, que incluem também pessoas tatuadas.[29] O rastreio é igualmente recomendado em indivíduos com níveis elevados de enzimas, já que este é normalmente o único indício de hepatite crónica.[35]
Prevenção[edit]
À data de 2011, não existe ainda qualquer vacina que ofereça protecção contra a contracção da hepatite C. No entanto, existem algumas em fase de desenvolvimento que mostram resultados promissores.[36] A aplicação de múltiplas medidas de contenção, como os programas de troca de seringas e o tratamento da toxicodependência, reduzem o risco da transmissão do vírus entre toxicodependentes em cerca de 75%.[37] O rastreio de dadores de sangue é importante quando feito à escala nacional, assim como o é a adesão das unidades de saúde aos princípios básicos de precaução, como a esterilização.[10] Em países onde não haja quantidade suficiente de seringas esterilizadas, a administração de medicamentos deve ser feita oralmente em vez de por via intravenosa.[12]
Tratamento[edit]
O VHC induz infecção crónica em 50% a 80% dos indivíduos infectados. Entre estes, a taxa de sucesso do tratamento é de 40% a 80%.[38][39] Em casos raros, a infecção pode desaparecer sem qualquer tratamento.[7] Os portadores de hepatite C crónica são aconselhados a evitar bebidas alcoólicas e medicamentos que apresentem toxicidade para o fígado,[6] para além de ser recomendada a vacinação contra a hepatite A e hepatite B.[6] Para aqueles que têm cirrose, recomenda-se também a vigilância do hepatocarcinoma através de ecografia.[6]
Medicação[edit]
Regra geral, recomenda-se o tratamento para todos aqueles em que se sejam detectadas anormalidades no fígado como resultado da infecção de VHC.[6] Actualmente, o tratamento é a administração combinada de interferão alfa peguilado com o fármaco antiviral ribavirina durante um período de 24 ou 48 semanas, dependendo do genótipo do VHC.[6] Quando administrado em conjunto com a ribavirina, o interferão alfa peguilado 2a aparenta superior ao interferão alfa peguilado 2b, embora as provas não sejam ainda determinantes.[40] Registam-se melhorias em 50% a 60% dos pacientes.[6] A combinação de boceprevri ou telaprevir com a ribavirina e e o interferão alfa peguilado melhora a resposta antiviral ao genótipo 1 da hepatite c.[41][42][43] Os efeitos secundários deste tratamento são bastante comuns, com cerca de metade dos pacientes a manifestarem sintomas semelhantes aos da gripe e cerca de um terço a manifestar problemas de ordem emocional.[6] O tratamento durante os primeiros seis meses é mais eficaz do que aquele que seja feito depois da infecção se ter tornado crónica.[13] Se o indivíduo contrair uma nova infecção e esta não tiver sido eliminada ao fim de oito a doze semanas, é recomendada a administração de interferão peguilado durante 24 semanas.[13] Em pacientes com talassemia, a ribavirina aparenta ser eficaz, mas aumenta a necessidade de transfusões.[44]
Medicina alternativa[edit]
Existem várias terapias alternativas cujos proponentes advogam ser benéficas no tratamento da hepatite C, como o cardo-leiteiro, ginseng ou a prata.[45] No entanto, nenhuma terapia alternativa mostrou ainda ser capaz de melhorar os resultados da doença, e não existe qualquer evidência de que as terapias alternativas tenham qualquer acção sobre o vírus.[45][46][47]
Prognóstico[edit]
A resposta ao tratamento varia consoante o genótipo do vírus. A resposta é positiva em 40% a 50% dos indivíduos infectados com o genótipo 1 depois de 48 semanas de tratamento.[4] Em indivíduos infectados com o genótipo 2, a resposta é positiva em 70% a 80% dos casos após 24 semanas de tratament.[4] Para o genótipo 4 a resposta positiva é de 65% após 48 semanas de tratamento. As evidências para o tratamento do genótipo 6 são escasssas, e as que existem são apenas para 48 semanas de tratamento com a mesma dosagem usada nos casos de genótipo 1.[48]
Epidemiologia[edit]

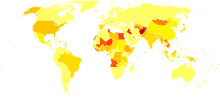
| sem dados <10 10-15 15-20 20-25 25-30 30-35 | 35-40 40-45 45-50 50-75 75–100 >100 |
Estima-se que vivam entre 130 e 170 milhões de pessoas com hepatite C crónica, o que corresponde a 3% da população mundial.[49] Anualmente, são registados 3 a 4 milhões de novos casos, e mais de 350.000 pessoas morrem a cada ano devido a doenças relacionadas com a hepatite C.[49] O número de infecções cresceu significativamente ao longo do século XX como consequência do contágio relativo ao consumo de drogas injectáveis, medicação intravenosa ou equipamento médico mal esterilizado.[12]
Entre os portadores crónicos da doença, o risco de contrair cirrose durante um prazo de vinte anos varia consoante os estudos efectuados, mas estima-se que seja entre 10% e 15% para os homens e entre 1% e 5% para as mulheres. Desconhece-se a explicação para esta diferença. Uma vez contraída cirrose, o taxa de risco de contrair hepatocarcinoma é de 1% a 4% ao ano.[50]
Nos Estados Unidos, cerca de 2% da população é portadora do vírus da hepatite C,[6] e anualmente são registados de 35.000 a 185.000 novos casos. A taxa de novas infecções tem vindo a diminuir de forma significativa no Ocidente desde a década de 1990 como consequência do rastreio de sangue em transfusões.[13] As mortes anuais devidas ao VHC nos Estados Unidos variam entre 8000 a 10000, esperando-se que este número aumente à medida que são registados as manifestações da doença em indivíduos infectados antes dos rastreios sanguíneos serem norma.[51]
A prevalência é maior em alguns países de África e da Ásia.[52] Entre os países com uma taxa significativamente elevada de infecções conta-se o Egipto (22%), o Paquistão (4,8%) e a China (3,2%).[49] Acredita-se que o caso Egípiio esteja ligado a uma campanha nacional para o tratamento da esquistossomose, actualmente descontinuada, em que foram usadas seringas de vidro esterilizadas de forma imprópria.[12]
História[edit]
Em meados da década de 1970, Harvey J. Alter, coordenador da Secção de Doenças Infecciosas no Departamento de Medicina de Transfusão nos Institutos Nacionais da Saúde, e a sua equipa de investigação demonstraram que a maior parte dos casos de hepatite registados após transfusões de sangue não se deviam aos vírus quer da hepatite A quer da B. Apesar desta descoberta e do esforço internacional para a identificação do vírus, inicialmente descrito como "vírus da hepatite não-A e não-B", tal só seria conseguido mais de uma década depois. Em 1987, Michael Houghton, Qui-Lim Choo, e George Kuo da Chiron Corporation, em colaboração com D.W. Bradley do Centro de Controle e Prevenção de Doenças, recorreram a uma nova abordagem baseada na clonagem molecular de modo a identificar o organismo ainda desconhecido e criar um teste de diagnóstico.[53] Em 1988, a existência do vírus foi confirmada por Alter ao verificar a sua presença numa cultura de vírus não-A e não-B. Em Abril de 1989, a descoberta do VHC foi publicada ao longo de dois artigos na revista Science.[54][55] A descoberta veio permitir melhorias substanciais no diagnóstico e no tratamento antiviral.[53] Em 2000, Alter e Houghton froam laureados com o Prémio Lasker para a Investigação Clínica em Medicina, pelo seu trabalho de pioneirismo na descoberta do vírus da hepatite C e pelo desenvolvimento de métodos de diagnóstico, que reduziram o risco de hepatite associada à transfusão de sangue nos Estados Unidos de 30% em 1970 para virtualmente zero em 2000.[56]
A Chiron deu entrada de vários pedidos de patente sobre o vírus e respectivos métodos de diagnóstico.[57] Em 1990, a CDC desistiu de registar uma patente concorrente, depois da Chiron ter oferecido uma indemnização no valor de 1,9 milhões de dólares à empresa e 337.500 dólares a Bradley. Em 1994, o próprio Bradley processou a Chiron, procurando invalidar a patente, incluir-se a si como co-autor e obter o direito a royalties. Viria, no entanto, a desistir do caso em 1998 depois de ter perdido num tribunal de recurso.[58]
Impacto social[edit]
Em 28 de Julho de cada ano celebra-se o Dia Mundial de Combate à Hepatite.[59] O impacto económico da hepatite C é bastante significativo, quer a nível individual, quer a nível social. Nos Estados Unidos, o custo médio da doença ao longo da vida foi estimado em 33.407 dólares em 2003,[60] e o custo de um transplante hepático em 200.000 dólares em 2011.[61] No Canadá, o custo de um tratamento antiviral ascendia em 2003 a 20.000 CAD,[62] e nos Estados Unidos entre 9200 e 17600 dólares em 1998.[60] Em muitas regiões do mundo, torna-se impossível comportar o tratamento com antivirais, quer por falta de seguro de saúde, quer pelo tratamento antiviral não estar coberto pela apólice.[63]
Investigação[edit]
À data de 2011, existem cerca de cem fármacos para a hepatite C em fase de desenvolvimento.[61] Entre eles encontram-se vacinas, imunomoduladores e inibidores de ciclofilina.[64] Estas inovações e potenciais tratamentos são resultado da melhor compreensão do vírus da hepatite C.[65]
References[edit]
- ^ a b Ryan KJ, Ray CG (editors), ed. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 551–2. ISBN 0838585299.
{{cite book}}:|editor=has generic name (help) - ^ Houghton M (November 2009). "The long and winding road leading to the identification of the hepatitis C virus". Journal of Hepatology. 51 (5): 939–48. doi:10.1016/j.jhep.2009.08.004. PMID 19781804.
{{cite journal}}: CS1 maint: date and year (link) - ^ Shors, Teri (2011-11-08). Understanding viruses (2nd ed.). Burlington, MA: Jones & Bartlett Learning. p. 535. ISBN 9780763785536.
- ^ a b c d e f g h i j k Rosen, HR (2011-06-23). "Clinical practice. Chronic hepatitis C infection" (PDF). The New England Journal of Medicine. 364 (25): 2429–38. doi:10.1056/NEJMcp1006613. PMID 21696309.
- ^ Maheshwari, Anurag; Ray, Stuart; Thuluvath, Paul J. (2008-07-26). "Acute hepatitis C". Lancet. 372 (9635): 321–32. doi:10.1016/S0140-6736(08)61116-2. PMID 18657711.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ a b c d e f g h i j k l m n o p q r s t Wilkins, T.; Malcolm, J. K.; Raina, D.; Schade, R. R. (2010-06-01). "Hepatitis C: diagnosis and treatment" (PDF). American Family Physician. 81 (11): 1351–7. PMID 20521755.
- ^ a b c d e Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future. Springer Verlag. 2011. p. 4. ISBN 9781461411918.
- ^ a b c d Nelson, Paul K.; Mathers, Bradley M.; Cowie, Benjamin; Hagan, Holly; Des Jarlais, Don; Horyniak, Danielle; Degenhardt, Louisa (2011-08-13). "Global epidemiology of hepatitis B and hepatitis C in people who inject drugs: results of systematic reviews". Lancet. 378 (9791): 571–83. doi:10.1016/S0140-6736(11)61097-0. PMC 3285467. PMID 21802134.
- ^ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future. Springer Verlag. 2011. pp. 103–104. ISBN 9781461411918.
- ^ a b c d e f g Ray, Stuart C.; Thomas, David L. (2009). "Chapter 154: Hepatitis C". In Mandell, Gerald L.; Bennett, John E.; Dolin, Raphael (eds.). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (7th ed.). Philadelphia, PA: Churchill Livingstone. ISBN 978-0443068393.
- ^ Mueller, S.; Millonig, G.; Seitz, H. K. (2009-07-28). "Alcoholic liver disease and hepatitis C: a frequently underestimated combination" (PDF). World Journal of Gastroenterology : WJG. 15 (28): 3462–71. doi:10.3748/wjg.15.3462. PMC 2715970. PMID 19630099.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ a b c d e f g h i j Alter, MJ (2007-05-07). "Epidemiology of hepatitis C virus infection" (PDF). World Journal of Gastroenterology : WJG. 13 (17): 2436–41. doi:10.3748/wjg.v13.i17.2436. PMC 4146761. PMID 17552026.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ a b c d e Ozaras, Resat; Tahan, Veysel (2009). "Acute hepatitis C: prevention and treatment". Expert Review of Anti-infective Therapy. 7 (3): 351–61. doi:10.1586/eri.09.8. PMID 19344247.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Zignego, AL; Ferri, C; Pileri, SA; et al. (January 2007). "Extrahepatic manifestations of Hepatitis C Virus infection: a general overview and guidelines for a clinical approach". Digestive and Liver Disease. 39 (1): 2–17. doi:10.1016/j.dld.2006.06.008. PMID 16884964.
{{cite journal}}: CS1 maint: date and year (link) - ^ Louie, K. S.; Micallef, J. M.; Pimenta, J. M.; Forssen, U. M. (2011). "Prevalence of thrombocytopenia among patients with chronic hepatitis C: a systematic review". Journal of Viral Hepatitis. 18 (1): 1–7. doi:10.1111/j.1365-2893.2010.01366.x. PMID 20796208.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Lee, Michael R.; Shumack, Stephen (2005). "Prurigo nodularis: a review". The Australasian Journal of Dermatology. 46 (4): 211–18, quiz 219–20. doi:10.1111/j.1440-0960.2005.00187.x. PMID 16197418.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Iannuzzella, F; Vaglio, A; Garini, G (May 2010). "Management of hepatitis C virus-related mixed cryoglobulinemia". Am. J. Med. 123 (5): 400–8. doi:10.1016/j.amjmed.2009.09.038. PMID 20399313.
{{cite journal}}: CS1 maint: date and year (link) - ^ Nakano, T; Lau, GM; Lau, GM; et al. (December 2011). "An updated analysis of hepatitis C virus genotypes and subtypes based on the complete coding region". Liver Int. 32 (2): 339–45. doi:10.1111/j.1478-3231.2011.02684.x. PMID 22142261.
{{cite journal}}: CS1 maint: date and year (link) - ^ Maheshwari, Anurag; Thuluvath, Paul J. (2010). "Management of acute hepatitis C". Clinics in Liver Disease. 14 (1): 169–76, x. doi:10.1016/j.cld.2009.11.007. PMID 20123448.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ a b c d e Pondé, RA (February 2011). "Hidden hazards of HCV transmission". Medical Microbiology and Immunology. 200 (1): 7–11. doi:10.1007/s00430-010-0159-9. PMID 20461405.
{{cite journal}}: CS1 maint: date and year (link) - ^ a b Xia, X.; Luo, J.; Bai, J.; Yu, R. (2008). "Epidemiology of HCV infection among injection drug users in China: systematic review and meta-analysis". Public Health. 122 (10): 990–1003. doi:10.1016/j.puhe.2008.01.014. PMID 18486955.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Imperial, JC (June 2010). "Chronic hepatitis C in the state prison system: insights into the problems and possible solutions". Expert Review of Gastroenterology & Hepatology. 4 (3): 355–64. doi:10.1586/egh.10.26. PMID 20528122.
{{cite journal}}: CS1 maint: date and year (link) - ^ Vescio, M. F.; Longo, B.; Babudieri, S.; Starnini, G.; Carbonara, S.; Rezza, G.; Monarca, R. (2008). "Correlates of hepatitis C virus seropositivity in prison inmates: a meta-analysis". Journal of Epidemiology and Community Health. 62 (4): 305–13. doi:10.1136/jech.2006.051599. PMID 18339822.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Day RA; Paul P; Williams B; et al. (November 2009). Brunner & Suddarth's textbook of Canadian medical-surgical nursing (Canadian 2nd ed.). Philadelphia, PA: Lippincott Williams & Wilkins. p. 1237. ISBN 9780781799898.
{{cite book}}: Explicit use of et al. in:|author=(help)CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ a b Marx, John (2010). Rosen's emergency medicine: concepts and clinical practice 7th edition. Philadelphia, PA: Mosby/Elsevier. p. 1154. ISBN 9780323054720.
- ^ "Highest Rates of Hepatitis C Virus Transmission Found in Egypt". Al Bawaaba. 2010-08-09. Retrieved 2010-08-27.
- ^ a b c Tohme RA, Holmberg SD (June 2010). "Is sexual contact a major mode of hepatitis C virus transmission?". Hepatology. 52 (4): 1497–505. doi:10.1002/hep.23808. PMID 20635398.
{{cite journal}}: CS1 maint: date and year (link) - ^ "Hepatitis C Group Education Class". United States Department of Veteran Affairs.
- ^ a b c d e f Jafari, Siavash; Copes, Ray; Baharlou, Souzan; Etminan, Mahyar; Buxton, Jane (2010). "Tattooing and the risk of transmission of hepatitis C: a systematic review and meta-analysis" (PDF). International Journal of Infectious Diseases : IJID : Official Publication of the International Society for Infectious Diseases. 14 (11): e928–40. doi:10.1016/j.ijid.2010.03.019. PMID 20678951.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ "Hepatitis C" (PDF). Centers for Disease Control and Prevention (CDC). Retrieved 2 January 2012.
- ^ Lock G; Dirscherl M; Obermeier F; et al. (September 2006). "Hepatitis C — contamination of toothbrushes: myth or reality?". J. Viral Hepat. 13 (9): 571–3. doi:10.1111/j.1365-2893.2006.00735.x. PMID 16907842.
{{cite journal}}: Unknown parameter|author-separator=ignored (help)CS1 maint: date and year (link) - ^ a b c "Hepatitis C FAQs for Health Professionals". Centers for Disease Control and Prevention (CDC). Retrieved 2 January 2012.
- ^ a b Lam, N. C.; Gotsch, P. B.; Langan, R. C. (2010-11-15). "Caring for pregnant women and newborns with hepatitis B or C" (PDF). American Family Physician. 82 (10): 1225–9. PMID 21121533.
- ^ Mast EE (2004). "Mother-to-infant hepatitis C virus transmission and breastfeeding". Advances in Experimental Medicine and Biology. 554: 211–6. doi:10.1007/978-1-4757-4242-8_18. ISBN 978-1-4419-3461-1. PMID 15384578.
- ^ Senadhi, V (July 2011). "A paradigm shift in the outpatient approach to liver function tests". Southern Medical Journal. 104 (7): 521–5. doi:10.1097/SMJ.0b013e31821e8ff5. PMID 21886053.
{{cite journal}}: CS1 maint: date and year (link) - ^ Halliday, John; Klenerman, Paul; Barnes, Eleanor (2011 May). "Vaccination for hepatitis C virus: closing in on an evasive target". Expert Review of Vaccines. 10 (5): 659–72. doi:10.1586/erv.11.55. PMC 3112461. PMID 21604986.
{{cite journal}}: Check date values in:|date=(help) - ^ Hagan, H.; Pouget, E. R.; Des Jarlais, D. C. (2011-07-01). "A systematic review and meta-analysis of interventions to prevent hepatitis C virus infection in people who inject drugs". The Journal of Infectious Diseases. 204 (1): 74–83. doi:10.1093/infdis/jir196. PMC 3105033. PMID 21628661.
- ^ Torresi, Joseph; Johnson, Doug; Wedemeyer, Heiner (2011). "Progress in the development of preventive and therapeutic vaccines for hepatitis C virus" (PDF). Journal of Hepatology. 54 (6): 1273–85. doi:10.1016/j.jhep.2010.09.040. PMID 21236312.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Ilyas, Jawad A.; Vierling, John M. (2011). "An overview of emerging therapies for the treatment of chronic hepatitis C". Clinics in Liver Disease. 15 (3): 515–36. doi:10.1016/j.cld.2011.05.002. PMID 21867934.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Awad T, Thorlund K, Hauser G, Stimac D, Mabrouk M, Gluud C (April 2010). "Peginterferon alpha-2a is associated with higher sustained virological response than peginterferon alfa-2b in chronic hepatitis C: systematic review of randomized trials". Hepatology. 51 (4): 1176–84. doi:10.1002/hep.23504. PMID 20187106.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Foote BS, Spooner LM, Belliveau PP (September 2011). "Boceprevir: a protease inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother. 45 (9): 1085–93. doi:10.1345/aph.1P744. PMID 21828346.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Smith LS, Nelson M, Naik S, Woten J (May 2011). "Telaprevir: an NS3/4A protease inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother. 45 (5): 639–48. doi:10.1345/aph.1P430. PMID 21558488.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB (October 2011). "An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases". Hepatology. 54 (4): 1433–44. doi:10.1002/hep.24641. PMC 3229841. PMID 21898493.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Alavian SM, Tabatabaei SV (April 2010). "Treatment of chronic hepatitis C in polytransfused thalassaemic patients: a meta-analysis". J. Viral Hepat. 17 (4): 236–44. doi:10.1111/j.1365-2893.2009.01170.x. PMID 19638104.
{{cite journal}}: CS1 maint: date and year (link) - ^ a b Hepatitis C and CAM: What the Science Says. National Center for Complementary and Alternative Medicine (NCCAM). March 2011. (Retrieved 7 March 2011)
- ^ Liu, Jianping; Manheimer, Eric; Tsutani, Kiichiro; Gluud, Christian (2003). "Medicinal herbs for hepatitis C virus infection: a Cochrane hepatobiliary systematic review of randomized trials". The American Journal of Gastroenterology. 98 (3): 538–44. doi:10.1111/j.1572-0241.2003.07298.x. PMID 12650784.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Rambaldi, A; Jacobs, BP; Gluud, C (2007-10-17). Rambaldi, Andrea (ed.). "Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases". Cochrane Database of Systematic Reviews. 2007 (4). CD003620 (2nd rev.). doi:10.1002/14651858.CD003620.pub2. PMC 8724782. PMID 17943794.
{{cite journal}}: External link in|coauthors=|coauthors=ignored (|author=suggested) (help) - ^ Fung J; Lai CL; Hung I; et al. (September 2008). "Chronic hepatitis C virus genotype 6 infection: response to pegylated interferon and ribavirin". The Journal of Infectious Diseases. 198 (6): 808–12. doi:10.1086/591252. PMID 18657036.
{{cite journal}}: Unknown parameter|author-separator=ignored (help)CS1 maint: date and year (link) - ^ a b c "Hepatitis C". World Health Organization (WHO). June 2011. Retrieved 2011-07-13.
{{cite web}}: CS1 maint: date and year (link) - ^ Yu, Ming-Lung; Chuang, Wan-Long (2009). "Treatment of chronic hepatitis C in Asia: when East meets West". J. Gastroenterol. Hepatol. 24 (3): 336–45. doi:10.1111/j.1440-1746.2009.05789.x. PMID 19335784.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Blatt, L. M.; Tong, M. (2004). Colacino, J. M.; Heinz, B. A. (eds.). Hepatitis prevention and treatment. Basel: Birkhäuser. p. 32. ISBN 9783764359560.
- ^ Holmberg, Scott. Brunette, Gary W.; Kozarsky, Phyllis E.; Magill, Alan J.; Shlim, David R.; Whatley, Amanda D. (eds.). CDC Health Information for International Travel 2012. New York: Oxford University Press. p. 231. ISBN 9780199769018.
- ^ a b Boyer, JL (2001). Liver cirrhosis and its development: proceedings of the Falk Symposium 115. Springer. pp. 344. ISBN 9780792387602.
- ^ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (April 1989). "Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome". Science. 244 (4902): 359–62. doi:10.1126/science.2523562. PMID 2523562.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Kuo G; Choo QL; Alter HJ; et al. (April 1989). "An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis". Science. 244 (4902): 362–4. doi:10.1126/science.2496467. PMID 2496467.
{{cite journal}}: Unknown parameter|author-separator=ignored (help)CS1 maint: date and year (link) - ^ Winners Albert Lasker Award for Clinical Medical Research, The Lasker Foundation. Retrieved 20 February 2008.
- ^ EP patent 0318216, Houghton, M; Choo, Q-L & Kuo, G, "NANBV diagnostics", issued 1989-05-31, assigned to Chiron
- ^ Wilken, Judge. "United States Court of Appeals for the Federal Circuit". United States Court of Appeals for the Federal Circuit. Retrieved 11 January 2012.
- ^ Eurosurveillance editorial, team (2011-07-28). "World Hepatitis Day 2011" (PDF). Eurosurveillance. 16 (30). PMID 21813077.
- ^ a b Wong, JB (2006). "Hepatitis C: cost of illness and considerations for the economic evaluation of antiviral therapies". PharmacoEconomics. 24 (7): 661–72. doi:10.2165/00019053-200624070-00005. PMID 16802842.
- ^ a b El Khoury, AC; Klimack, WK; Wallace, C; Razavi, H (1 December 2011). "Economic burden of hepatitis C-associated diseases in the United States". Journal of Viral Hepatitis. 19 (3): 153–60. doi:10.1111/j.1365-2893.2011.01563.x. PMID 22329369.
- ^ "Hepatitis C Prevention, Support and Research ProgramHealth Canada". Public Health Agency of Canada. Nov 2003. Retrieved 10 January 2012.
{{cite web}}: CS1 maint: date and year (link) - ^ Zuckerman, edited by Howard Thomas, Stanley Lemon, Arie (2008). Viral Hepatitis (3rd ed.). Oxford: John Wiley & Sons. p. 532. ISBN 9781405143882.
{{cite book}}:|first=has generic name (help)CS1 maint: multiple names: authors list (link) - ^ Ahn, Joseph; Flamm, Steven L. (2011). "Hepatitis C therapy: other players in the game". Clinics in Liver Disease. 15 (3): 641–56. doi:10.1016/j.cld.2011.05.008. PMID 21867942.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link) - ^ Vermehren, J.; Sarrazin, C. (2011). "New HCV therapies on the horizon". Clinical Microbiology and Infection : The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases. 17 (2): 122–34. doi:10.1111/j.1469-0691.2010.03430.x. PMID 21087349.
{{cite journal}}: Unknown parameter|month=ignored (help)CS1 maint: date and year (link)
