User:KatSorWit/sandbox
Wirusowe zapalenie wątroby typu C (WZW C) – choroba atakująca głównie wątrobę, powodowana przez wirusa zapalenia wątroby typu C (ang. HCV – hepatitis C virus).[1] WZW C często przebiega bezobjawowo, ale jego przewlekła postać może prowadzić do włóknienia wątroby, co po wielu latach może skutkować rozwinięciem się marskości wątroby. W niektórych przypadkach osoby chore na marskość wątroby cierpią także z powodu niewydolności wątroby, raka wątroby, a także żylaków przełyku i żołądka, które mogą powodować śmiertelne krwotoki.[1]
Do zakażeń WZW C u ludzi dochodzi głównie przez kontakt krwi z krwią wśród osób przyjmujących dożylnie narkotyki, poprzez korzystanie z niejałowego sprzętu medycznego oraz podczas transfuzji krwi. Szacuje się, że na WZW C cierpi od 130 do 170 milionów osób na całym świecie. Naukowcy rozpoczęli prace nad badaniem wirusa HCV już w latach 70-tych XX wieku, a jego istnienie potwierdzili w roku 1989.[2] Przypadki zachorowań wśród zwierząt są nieznane.
Standardowymi lekami przeciwko wirusowi HCV są peginterferon oraz rybawiryna. Spośród osób poddawanych leczeniu wyleczonych zostaje 50-80%. U chorych, u których rozwinie się marskość lub rak wątroby, konieczny może być przeszczep wątroby, po którym jednak wirus najczęściej powraca.[3] Nie istnieje bowiem żadna szczepionka przeciwko WZW C.
Objawy i symptomy[edit]
WZW C tylko w 15% przypadków wywołuje ostre objawy zakażenia.[4] Znacznie częściej symptomy są łagodne i nieoczywiste, a zalicza się do nich zmniejszenie apetytu, zmęczenie, mdłości, bóle mięśniowo-stawowe oraz utratę wagi.[5] Tylko nieliczne przypadki ostrej fazy infekcji mają związek z żółtaczką.[6] WZW C ustępuje bez leczenia u 10-50% osób, najczęściej młodych kobiet.[6]
Faza przewlekła[edit]
U osiemdziesięciu procent osób, które miały styczność z wirusem, infekcja przechodzi w stan przewlekły.[7] Podczas pierwszych kilkudziesięciu lat choroby objawy u większości z nich są nieznaczne lub całkiem ich brak,[8] choć stan przewlekły może powodować uczucie zmęczenia.[9] WZW C jest główną przyczyną występowania marskości wątroby oraz raka wątroby wśród osób żyjących z zakażeniem od wielu lat.[3] W przypadku 10-30% osób żyjących z chorobą przez ponad 30 lat dochodzi do rozwoju marskości wątroby,[3][5] która częściej występuje u osób dodatkowo zakażonych wirusem WZW B lub HIV, u alkoholików i osób płci męskiej.[5] Osoby, u których dochodzi do marskości wątroby, są 20 razy bardziej narażone na ryzyko zachorowania na raka wątroby(wskaźnik zachorowań na poziomie 1-3% rocznie).[3][5] W przypadku alkoholików ryzyko jest 100 razy większe.[10] WZW C jest przyczyną 27% przypadków marskości wątroby i 25% raka wątroby.[11]
Marskość wątroby może prowadzić do wysokiego ciśnienia krwi w żyłach prowadzących do wątroby, nagromadzenia płynu w brzuchu, łatwego powstawania siniaków lub występowania krwawienia, powiększania się żył, szczególnie w przełyku, żółtaczki (zżółknienia skóry) oraz uszkodzenia mózgu.[12]
Objawy pozawątrobowe[edit]
W rzadkich przypadkach WZW C powoduje zespół Sjögrena (zaburzenie autoimmunologiczne), obniżenie poziomu płytek krwi, przewlekłą chorobę skóry, cukrzycę oraz chłoniaki nieziarniczne.[13][14]
Etiologia[edit]
Wirus zapalenia wątroby typu C to mały, otoczkowy, jednoniciowy wirus RNA o dodatniej polarności (+ssRNA-wirus),[3] który należy do rodzaju Hepacivirus w rodzinie Flaviviridae.[9] Występuje siedem głównych genotypów wirusa HCV.[15] W USA podtyp 1 jest przyczyną 70% zachorowań, podtyp 2 20% przypadków, a każdy następny podtyp powoduje 1% zakażeń.[5] Genotyp 1 jest także najczęściej występującym w Ameryce Południowej oraz w Europie.[3]
Rozprzestrzenianie się choroby[edit]
Główną drogą rozprzestrzeniania się choroby w krajach rozwiniętych jest dożylne zażywanie narkotyków (ang. IDU – intravenous drug use), zaś w krajach rozwijających się choroba najczęściej roznosi się podczas transfuzji krwi oraz wykonywania procedur medycznych, podczas których nie stosuje się środków bezpieczeństwa.[16] W 20% przypadków źródła zakażenia są nieznane,[17] ale wiele z nich można przypisać IDU.[6]
Dożylne zażywanie narkotyków[edit]
Dożylne przyjmowanie narkotyków to główny czynnik ryzyka występowania WZW C w wielu krajach świata.[18] Badania przeprowadzone w 77 państwach wykazały, że w 25 z nich wskaźnik zachorowań na WZW C wśród populacji przyjmującej dożylnie narkotyki wynosi 60-80%, co dotyczy także USA[7] oraz Chin. [18] W 12 krajach wskaźnik ten przekracza 80%.[7] Aż 10 milionów osób przyjmujących narkotyki przez iniekcje jest zakażonych WZW C, z czego najwyższa liczba zachorowań występuje w Chinach (1,6 milionów), USA (1,5 milionów) oraz Rosji (1,3 milionów).[7] Wskaźnik zakażeń WZW C wśród więźniów w USA wynosi 10 do 20 przypadków w porównaniu z populacją ogólną, co badania przypisują zachowaniom wysokiego ryzyka, takim jak IDU oraz tatuowanie się niesterylnym sprzętem.[19][20]
====Zakażenia związane z opieką zdrowotną==== Transfuzje krwi, produkty krwiopochodne oraz przeszczepy organów wykonywane bez przeprowadzania badań przesiewowych pod kątem obecności wirusa HCV są źródłem znacznego ryzyka zakażenia.[5] Odkąd w USA wprowadzono w 1992 roku rutynowe badania przesiewowe wskaźnik zakażeń spadł z 1:200 jednostek krwi do 1:10 000 i w końcu do 1:10 000 000 jednostek krwi.[21] To niskie ryzyko utrzymuje się, ponieważ przedział czasu od chwili zakażenia się dawcy krwi WZW C do momentu, gdy test laboratoryjny wskaże wynik pozytywny, wynosi około 11-70 dni (tzw. okienko serologiczne).[17] Niektóre kraje nadal nie prowadzą badań przesiewowych pod kątem WZW C z uwagi na ich koszt.[11]
W przypadku osoby, która przypadkowo zakłuje się igłą używaną wcześniej na chorym z WZW C, istnieje 1,8% szans, że dojdzie do zakażenia.[5] Ryzyko jest większe, gdy zakłuto się igłą iniekcyjną (z kanalikiem) oraz gdy rana jest głęboka.[11] Niewielkim zagrożeniem zakażenia jest kontakt śluzu z krwią, natomiast żadne ryzyko nie występuje podczas styczności krwi z nienaruszoną powierzchnią skóry.[11]
Sprzęt szpitalny może także powodować rozprzestrzenianie się WZW C poprzez m.in.: wielokrotne korzystanie z tych samych igieł i strzykawek, wielorazowe fiolki na leki, worki infuzyjne oraz niejałowe instrumenty chirurgiczne.[11] Niskie standard higieny w ośrodkach medycznych i stomatologicznych są główną przyczyną rozprzestrzeniania się wirusa HCV w Egipcie – kraju z najwyższym wskaźnikiem zakażeń na świecie.[22]
Stosunki seksualne[edit]
Niewiadomo, czy WZW C może być przenoszone drogą płciową.[23] O ile istnieje związek między czynnościami seksualnymi wysokiego ryzyka a WZW C, o tyle niejasne jest, czy przenoszenie się choroby jest powodowane przez nieujawnione zażywanie narkotyków, czy samo uprawianie seksu.[5] Dowody pozwalają podtrzymywać stanowisko, że nie istnieje ryzyko zakażenia wśród par heteroseksualnych, które nie uprawiają seksu z innymi partnerami.[23] Natomiast czynności seksualne stanowiące ryzyko to takie, które powodują znaczne uszkodzenia mechaniczne w wewnętrznej wyściółce kanału odbytu, np. penetracja analna, lub które występują razem z chorobami przenoszonymi drogą płciową (wraz z HIV lub owrzodzeniem genitaliów).[23] Właściwa agencja rządowa USA zaleca jedynie stosowanie prezerwatyw, aby zapobiegać rozprzestrzenianiu się WZW C wśród osób, które mają wielu partnerów seksualnych.[24]
Kolczykowanie i tatuowanie ciała[edit]
Tatuowanie ciała zwielokrotnia ryzyko zarażenia o 2-3 razy.[25] Źródłem infekcji może być niejałowy sprzęt lub skażenie wykorzystywanych barwników.[25] Tatuaże lub przekłucia wykonane przed rokiem 1985 lub metodą chałupniczą są szczególnym powodem do niepokoju, ponieważ techniki sterylizacji mogły być wówczas słabe. Ponadto, ryzyko wystąpienia choroby jest proporcjonalne do wielkości tatuażu.[25] Ponad połowa wszystkich osadzonych korzysta z tego samego niewyjaławianego sprzętu do wykonywania tatuaży.[25] Rzadko zdarza się, aby tatuaż wykonany w autoryzowanym salonie, miał bezpośredni związek z zakażeniem wirusem HCV.[26]
Styczność z zakażoną krwią[edit]
Środki higieny osobistej, takie jak maszynki do golenia, szczoteczki do zębów, zestawy do manicure oraz pedicure mogą mieć styczność z krwią zakażonego. Współdzielenie ich z innymi naraża na kontakt z wirusem HCV.[27][28] Choć w przypadku skaleczeń oraz podrażnionych miejsc należy zachować ostrożność,[28] to wirus WZW C nie rozprzestrzenia się przez normalny kontakt, jak przytulanie, całowanie lub korzystanie z tym samych naczyń i sztućców.[28]
Przenoszenie pionowe z matki-nosicielki na dziecko[edit]
Przenoszenie się WZW C z matki-nosicielki na dziecko zdarza się rzadziej niż w 10% ciąż.[29] Nie istnieją żadne środki zaradcze, które obniżałyby to ryzyko.[29] Do zakażenia może dojść tak w czasie ciąży(wewnątrzmacicznie), jak i porodu (okołoporodowo).[17] Długi poród zwiększa ryzyko zarażenia dziecka.[11] Choć nie ma dowodów, że wirus HCV roznosi się przez karmienie piersią, to jednak zakażona matka powinna unikać karmienia piersią, jeśli jej brodawki są popękane i krwawią[30] lub jej miano wirusa jest wysokie.[17]
Metody diagnostyczne[edit]
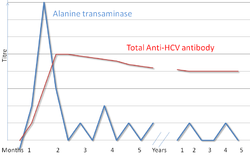
Rodzaje testów diagnostycznych w kierunku WZW C to: anty-HCV, test immunoenzymatyczny ELISA, test Western blot oraz test ilościowy HCV RNA.[5] Metodą PCR (ang. Polymerase chain reaction, polimerazowa reakcja łańcuchowa) można wykrywać RNA wirusa HCV już jeden do dwóch tygodni po zakażeniu, natomiast przeciwciała mogą powstawać i ujawniać się po znacznie dłuższym czasie.[12]
O przewlekłym WZW C mówimy, gdy wirus HCV utrzymuje się w organizmie przez ponad 6 miesięcy, co stwierdza się na podstawie obecność RNA wirusa we krwi zakażonego.[8] Z uwagi na to, że zakażenia przewlekłe zazwyczaj przebiegają bezobjawowo przez dziesiątki lat,[8] klinicyści często odkrywają chorobę podczas testów oceniających funkcje wątroby lub podczas okresowych badań przesiewowych pacjentów obarczonych zwiększonym ryzkiem zakażenia. Na podstawie badań laboratoryjnych nie można rozróżnić zakażeń ostrych od przewlekłych.[11]
Badanie krwi[edit]
Badanie związane z wirusowym zapaleniem wątroby typu C zazwyczaj zaczyna się od badania krwi, którego celem jest wykrycie obecności antyciał HCV przy użyciu enzymowego badania odporności. [5] Jeżeli wynik jest pozytywny, przeprowadza się drugie badanie w celu potwierdzenia badania odporności oraz określenia stopnia.[5] Rekombinant próby immunoblot używany jest do potwierdzenia badania na odporność, a dzięki polimerazie reakcji łańcuchowej HCV RNA możliwe jest ustalenie stopnia.[5] Brak RNA i pozytywny wynik próby immunoblot oznacza, osoba była w przeszłości zakażona, ale wyzdrowiała w wyniku leczenia lub samoistnie; jeżeli próba immunoblot dała wynik negatywny, badanie odporności wypadło źle. [5] Wynik badania odporności będzie pozytywny dopiero po okresie od sześciu do ośmiu tygodni od zakażenia. [9]
W początkowej fazie zakażenia poziom enzymów w wątrobie jest zmienny;[8] zazwyczaj zaczyna rosnąć po siedmiu tygodniach od zakażenia.[9] Enzymy w wątrobie nie mają związku ze stopniem choroby.[9]
Biopsja[edit]
Biopsja wątroby może pomóc określić stopień uszkodzenia wątroby, procedura wiąże się jednak z pewnym ryzykiem. [3] Typowe zmiany jakie można wykryć w drodze biopsji to obecność limfocytów w tkance wątroby, pęcherzyki limfoidalne w triadzie wtórnej oraz zmiany w przewodzie żółciowym.[3] Dostępnych jest wiele badań pozwalających określić stopień uszkodzenia zmniejszyć potrzebę przeprowadzenia biopsji.[3]
Badanie przesiewowe[edit]
W USA oraz Kanadzie zaledwie 5–50% zakażonych wie o swojej chorobie.[25] Osobom należącym do grup podwyższonym ryzyku, włącznie z osobami, które mają tatuaże, zaleca się przeprowadzenie badać.[25] Badania przesiewowe zaleca się również osobom o podniesionym poziomie enzymów w wątrobie, ponieważ często jest to jedyny objaw przewlekłego wirusowego zapalenia wątroby.[31] Okresowych badań przesiewowych nie zaleca się w USA.[5]
Profilaktyka[edit]
W 2011 r. nie było jeszcze możliwości zaszczepienia się przeciwko wirusowemu zapaleniu wątroby typu C. Trwają obecnie prace nad szczepionkami, a rezultaty ich są bardzo zachęcające.[32] Połączenie strategii profilaktycznych takich jak programy wymiany igieł oraz terapie dla osób nadużywających substancji odurzających pozwala zmniejszyć ryzyko wirusowego zapalenia wątroby typu C wśród narkomanów dożylnych o około 75%.[33] Na szczeblu krajowym bardzo ważne są badania przesiewowe dawców krwi oraz stosowanie uniwersalnych środków zapobiegawczych w instytucjach opieki medycznej. [9] W krajach, w których brakuje sterylnych strzykawek zaleca się usługodawcom zastępowanie zastrzyków lekami doustnymi.[11]
Leczenie[edit]
HCV jest przyczyną przewlekłego zakażenia u 50–80% zakażonych. W prawie 40-80% tych przypadków udaje się powstrzymać to dzięki leczeniu.[34][35] W rzadkich przypadkach zakażenie może ustąpić bez leczenia.[6] Osoby cierpiące na przewlekłe wirusowe zapalenie wątroby typu C powinny unikać alkoholu oraz leków szkodliwych dla wątroby[5] oraz powinny skorzystać ze szczepień przeciwko wirusowemu zapaleniu wątroby typu A i wirusowemu zapaleniu wątroby typu B.[5] Osoby cierpiące na marskość wątroby powinny poddać się badaniom przy użyciu ultradźwięków w kierunku raka wątroby.[5]
Leki[edit]
Osoby, u których wykryto zakażenie HCV powinny skorzystać z leczenia. [5] Obecne leczenie wiąże się z podawaniem pegylowanego interferonu oraz przeciwwirusowego leku ribavirin przez okres 24 lub 48 tygodni, w zależności od typu HCV.[5] Poprawa następuje u 50–60% osób objętych leczeniem.[5] Połączenie bocepreviru lub telapreviru z ribavirinem i peginterferonem alfa poprawia reakcję przeciwwirusową na wirusowe zapalenie wątroby typu C genotypu 1.[36][37][38] Częste są efekty uboczne leczenia; połowa leczonych cierpi z powodu objawów przypominających grypę a jedna trzecia na problemy emocjonalne.[5] Leczenie w ciągu pierwszych sześciu miesięcy jest skuteczniejsze niż później, ponieważ wirusowe zapalenie wątroby typu C przekształca się w chorobę przewlekłą.[12] W razie ponownego zakażenia, jeżeli zakażenie nie zostanie wyeliminowane w okresie od ośmiu do dwunastu miesięcy zaleca się 24 tygodniową kurację pegylowanym interferonem.[12] W przypadku osób cierpiących na talasemię (zaburzenie krwi) przydatny wydaje się ribavirin, ale oznacza to zwiększenie potrzeby przeprowadzania transfuzji.[39] Zwolennicy twierdzą, że przy wirusowym zapaleniu wątroby typu C pomaga kilka alternatywnych sposobów leczenia włączając w to ostropest plamisty, żeń-szeń oraz koloidalne srebro.[40] Jednak nie stwierdzono, żeby jakikolwiek alternatywny sposób leczenia pomagał osiągnąć lepsze wyniki wśród osób cierpiących na wirusowe zapalenie wątroby typu C, a co więcej brak dowodów na to, że alternatywne sposoby leczenia mają jakikolwiek wpływ na wirusa.[40][41][42]
Prognoza[edit]
Reakcja na leczenie różni się w zależności od genotypu. Podtrzymana reakcja utrzymuje się u 40-50% zakażonych wirusowym zapaleniem wątroby typu C genotypu 1 przez okres 48 tygodni po leczeniu.[3] Podtrzymana reakcja utrzymuje się u 70-80% osób zakażonych HCV genotypu 2 i 3 przez okres 24 tygodni po leczeniu.[3] Podtrzymane wyniki utrzymują się u ok. 65% osób z genotypem 4 przez okres 48 tygodni po leczeniu. Dowody związane z leczeniem choroby genotypu 6 są obecnie rzadkie, ale wskazują na utrzymywanie się objawów przez 48 tygodni po leczeniu, przy takich samych dawkach jak przy chorobie genotypu 1.[43]
Epidemiologia[edit]

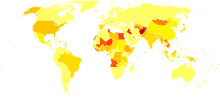
| no data <10 10-15 15-20 20-25 25-30 30-35 | 35-40 40-45 45-50 50-75 75–100 >100 |
Od 130 do 170 milionów ludzi lub ~3% populacji świata żyje z przewlekłym wirusowym zapaleniem wątroby typu C.[44] Około 3–4 milionów osób zaraża się nim co roku a ponad 350 000 osób umiera co roku w wyniku chorób związanych z wirusowym zapaleniem wątroby typu C.[44] Liczby te znacznie wzrosły w XX w. w wyniku narkotyków dożylnych oraz niesterylizowanego sprzętu medycznego.[11]
W USA na wirusowe zapalenie wątroby typu C cierpi ok. 2% populacji,[5] co roku zaraża się nim od 35 000 do 185 000 osób. Liczby te uległy zmniejszeniu w zachodnim świecie od lat 90 w wyniku usprawnienia badań przesiewowych krwi przed przeprowadzeniem transfuzji.[12] Co roku z powodu HCV umiera w USA od 8 000 do 10 000 osób. Oczekuje się, że liczba zgonów wzrośnie, ponieważ osoby zakażone w wyniku transfuzji wykonywanej przed wprowadzeniem badań w kierunku HCV zachorują i umrą.[45]
Częstotliwość zakażeń jest wyższa w niektórych państwach w Afryce oraz Azjii.[46] Państwa o najwyższym odsetku zakażeń to Egipt (22%), Pakistan (4,8%) oraz Chiny (3,2%).[44] Wysoki odsetek w Egipce ma związek z zaniechaną już masową kampanią przeciwko schistosomatozie, w której wykorzystywano nieprawidłowo sterylizowane szklane strzykawki.[11]
Historia[edit]
W połowie lat 70, Harvey J. Alter, szef Działu Chorób Zakaźnych na Wydziale Transfuzji w Krajowym Instytucie Zdrowia oraz jego zespół badawczy wykazali, że większość przypadków wirusowego zapalenia wątroby po transfuzji krwi nie wynikała z wirusowego zapalenia wątroby typu A lub B. Mimo tego odkrycia przez kolejną dekadę międzynarodowe badania na rzecz identyfikacji wirusa były nieskuteczne. W 1987 Michael Houghton, Qui-Lim Choo i George Kuo z Chiron Corporation we współpracy z dr D.W. Bradleyem z Centrum Kontroli oraz Profilaktyki Chorób wykorzystali nową metodę klonowania molekularnego do zidentyfikowania nieznanego organizmu oraz opracowania badań diagnostycznych.[47] W 1988 r. Alter potwierdził istnienie wirusa poprzez stwierdzenie jego obecności w próbce wirusowego zapalenia wątroby typu innego niż A i B. W kwietniu 1989 r. odkrycie HCV zostało opisane w dwóch artykułach opublikowanych na łamach magazynu Science.[48][49] Wspomniane odkrycie przyczyniło się do znacznego usprawnienia leczenie przeciwwirusowego.[47] W 2000 dr. Alter i Houghton zostali uhonorowani Nagrodą im. Alberta Laskera w dziedzinie klinicznych badań medycznych za "pionierskie prace prowadzące do odkrycia wirusa wywołującego wirusowe zapalenie wątroby typu C oraz opracowanie metod badań przesiewowych, które zmniejszyły ryzyko zakażenia wirusowym zapaleniem wątroby w wyniku transfuzji krwi w USA z 30% w 1970 roku prawie do zera w 2000 r."[50]
Firma Chiron złożyła podanie o przyznanie kilku patentów dotyczących wirusa oraz diagnostyki.[51] Konkurencyjne podanie o nadanie patentu CDC zostało odrzucone w 1990 po tym jak firma Chiron zapłaciła $1,9 miliona CDC oraz $337 500 Bradleyowi. W 1994 Bradley pozwał Chiron, próbując unieważnić patent i starając się o uzyskanie statusu współwynalazcy oraz licząc na rekompensatę i zysk tytułem honorarium. Zrezygnował ze swoich żądań w 1998 po tym jak przegrał sprawę przed sądem odwoławczym.[52]
Społeczeństwo i kultura[edit]
World Hepatitis Alliance koordynuje Światowy dzień wirusowego zapalenia wątroby odbywający się co roku 28 lipca.[53] Gospodarcze koszty wirusowego zapalenia wątroby typu C są znaczne zarówno dla osób prywatnych jak i dla społeczeństwa. W USA przeciętny koszt choroby, w ciągu życia pacjenta wynosi 33 407 dolarów w 2003 r.,[54] podczas gdy koszt przeszczepu wątroby wynosił, w 2011 r., około 200 000 dolarów. [55] W Kanadzie koszt leczenie przeciwwirusowego wynosił w 2003 r. aż 30 000 dolarów kanadyjskich, [56] podczas gdy ten sam koszt w USA wahał się w 1998 r. od 9 200 do 17 600 dolarów. [54] W wielu rejonach świata ludzi nie stać na opłacenie leczenia przeciwwirusowego ze względu na brak ubezpieczenia lub to, że ich ubezpieczenie nie obejmuje leczenia przeciwwirusowego.[57]
Badania[edit]
W 2011 opracowywano ponad 100 leków na wirusowe zapalenie wątroby typu C.[55] Wśród leków tych były między innymi szczepionki przeciw wirusowemu zapaleniu wątroby, immunomodulatory oraz inhibitory cyclofilinowe.[58] Te potencjalne, nowe leki są rezultatem pełniejszego zrozumienia istoty wirusowego zapalenia wątroby typu C.[59]
Bibliografia[edit]
- ^ a b Ryan KJ, Ray CG (editors), ed. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 551–2. ISBN 0838585299.
{{cite book}}:|editor=has generic name (help) - ^ Houghton M (November 2009). "The long and winding road leading to the identification of the hepatitis C virus". Journal of Hepatology. 51 (5): 939–48. doi:10.1016/j.jhep.2009.08.004. PMID 19781804.
{{cite journal}}: CS1 maint: date and year (link) - ^ a b c d e f g h i j k Rosen, HR (2011-06-23). "Clinical practice. Chronic hepatitis C infection" (PDF). The New England Journal of Medicine. 364 (25): 2429–38. doi:10.1056/NEJMcp1006613. PMID 21696309.
- ^ Maheshwari, Anurag; Ray, Stuart; Thuluvath, Paul J. (2008-07-26). "Acute hepatitis C.". Lancet. 372 (9635): 321–32. doi:10.1016/S0140-6736(08)61116-2. PMID 18657711.
- ^ a b c d e f g h i j k l m n o p q r s t u v Wilkins, T.; Malcolm, J. K.; Raina, D.; Schade, R. R. (2010-06-01). "Hepatitis C: diagnosis and treatment". American Family Physician. 81 (11): 1351–7. PMID 20521755.
- ^ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future. Springer Verlag. 2011. p. 4. ISBN 9781461411918.
- ^ a b c d Nelson, Paul K.; Mathers, Bradley M.; Cowie, Benjamin; Hagan, Holly; Des Jarlais, Don; Horyniak, Danielle; Degenhardt, Louisa (2011-08-13). "Global epidemiology of hepatitis B and hepatitis C in people who inject drugs: results of systematic reviews". Lancet. 378 (9791): 571–83. doi:10.1016/S0140-6736(11)61097-0. PMC 3285467. PMID 21802134.
- ^ a b c d Chronic Hepatitis C Virus Advances in Treatment, Promise for the Future. Springer Verlag. 2011. pp. 103–104. ISBN 9781461411918.
- ^ a b c d e f Dolin, [edited by] Gerald L. Mandell, John E. Bennett, Raphael (2010). Mandell, Douglas, and Bennett's principles and practice of infectious diseases (7th ed.). Philadelphia, PA: Churchill Livingstone/Elsevier. pp. Chapter 154. ISBN 978-0443068393.
{{cite book}}:|first=has generic name (help)CS1 maint: multiple names: authors list (link) - ^ Mueller, S.; Millonig, G.; Seitz, H. K. (2009-07-28). "Alcoholic liver disease and hepatitis C: a frequently underestimated combination". World Journal of Gastroenterology : WJG. 15 (28): 3462–71. doi:10.3748/wjg.15.3462. PMC 2715970. PMID 19630099.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ a b c d e f g h i j Alter, MJ (2007-05-07). "Epidemiology of hepatitis C virus infection". World Journal of Gastroenterology : WJG. 13 (17): 2436–41. doi:10.3748/wjg.v13.i17.2436. PMC 4146761. PMID 17552026.
{{cite journal}}: CS1 maint: unflagged free DOI (link) - ^ a b c d e Ozaras, R.; Tahan, V. (2009 Apr). "Acute hepatitis C: prevention and treatment". Expert Review of Anti-infective Therapy. 7 (3): 351–61. doi:10.1586/eri.09.8. PMID 19344247.
{{cite journal}}: Check date values in:|date=(help) - ^ Zignego AL, Ferri C, Pileri SA, Caini P, Bianchi FB (January 2007). "Extrahepatic manifestations of Hepatitis C Virus infection: a general overview and guidelines for a clinical approach". Digestive and Liver Disease. 39 (1): 2–17. doi:10.1016/j.dld.2006.06.008. PMID 16884964.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Louie, K. S.; Micallef, J. M.; Pimenta, J. M.; Forssen, U. M. (2011 Jan). "Prevalence of thrombocytopenia among patients with chronic hepatitis C: a systematic review". Journal of Viral Hepatitis. 18 (1): 1–7. doi:10.1111/j.1365-2893.2010.01366.x. PMID 20796208.
{{cite journal}}: Check date values in:|date=(help) - ^ Nakano T, Lau GM, Lau GM, Sugiyama M, Mizokami M (December 2011). "An updated analysis of hepatitis C virus genotypes and subtypes based on the complete coding region". Liver Int. 32 (2): 339–345. doi:10.1111/j.1478-3231.2011.02684.x. PMID 22142261.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Maheshwari, A.; Thuluvath, P. J. (2010 Feb). "Management of acute hepatitis C.". Clinics in Liver Disease. 14 (1): 169–76, x. doi:10.1016/j.cld.2009.11.007. PMID 20123448.
{{cite journal}}: Check date values in:|date=(help) - ^ a b c d Pondé, R. A. (2011 Feb). "Hidden hazards of HCV transmission". Medical Microbiology and Immunology. 200 (1): 7–11. doi:10.1007/s00430-010-0159-9. PMID 20461405.
{{cite journal}}: Check date values in:|date=(help) - ^ a b Xia, X (2008 Oct). "Epidemiology of HCV infection among injection drug users in China: systematic review and meta-analysis". Public Health. 122 (10): 990–1003. doi:10.1016/j.puhe.2008.01.014. PMID 18486955.
{{cite journal}}: Check date values in:|date=(help); Unknown parameter|coauthors=ignored (|author=suggested) (help) - ^ Imperial, JC (2010 Jun). "Chronic hepatitis C in the state prison system: insights into the problems and possible solutions". Expert Review of Gastroenterology & Hepatology. 4 (3): 355–64. doi:10.1586/egh.10.26. PMID 20528122.
{{cite journal}}: Check date values in:|date=(help) - ^ Vescio, M. F.; Longo, B.; Babudieri, S.; Starnini, G.; Carbonara, S.; Rezza, G.; Monarca, R. (2008 Apr). "Correlates of hepatitis C virus seropositivity in prison inmates: a meta-analysis". Journal of Epidemiology and Community Health. 62 (4): 305–13. doi:10.1136/jech.2006.051599. PMID 18339822.
{{cite journal}}: Check date values in:|date=(help) - ^ Marx, John (2010). Rosen's emergency medicine: concepts and clinical practice 7th edition. Philadelphia, PA: Mosby/Elsevier. p. 1154. ISBN 9780323054720.
- ^ "Highest Rates of Hepatitis C Virus Transmission Found in Egypt". Al Bawaba. 2010-08-09. Retrieved 2010-08-27.
- ^ a b c Tohme RA, Holmberg SD (June 2010). "Is sexual contact a major mode of hepatitis C virus transmission?". Hepatology. 52 (4): 1497–505. doi:10.1002/hep.23808. PMID 20635398.
{{cite journal}}: CS1 maint: date and year (link) - ^ "Hepatitis C Group Education Class". United States Department of Veteran Affairs.
- ^ a b c d e f Jafari, S.; Copes, R.; Baharlou, S.; Etminan, M.; Buxton, J. (2010 Nov). "Tattooing and the risk of transmission of hepatitis C: a systematic review and meta-analysis" (PDF). International Journal of Infectious Diseases : IJID : Official Publication of the International Society for Infectious Diseases. 14 (11): e928-40. doi:10.1016/j.ijid.2010.03.019. PMID 20678951.
{{cite journal}}: Check date values in:|date=(help) - ^ "Hepatitis C" (PDF). Center for Disease Control and Prevention. Retrieved 2 January 2012.
- ^ Lock G, Dirscherl M, Obermeier F; et al. (September 2006). "Hepatitis C —contamination of toothbrushes: myth or reality?". J. Viral Hepat. 13 (9): 571–3. doi:10.1111/j.1365-2893.2006.00735.x. PMID 16907842.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ a b c "Hepatitis C". FAQ – CDC Viral Hepatitis. Retrieved 2 Jan 2012.
- ^ a b Lam, N. C.; Gotsch, P. B.; Langan, R. C. (2010-11-15). "Caring for pregnant women and newborns with hepatitis B or C.". American Family Physician. 82 (10): 1225–9. PMID 21121533.
- ^ Mast EE (2004). "Mother-to-infant hepatitis C virus transmission and breastfeeding". Advances in Experimental Medicine and Biology. 554: 211–6. doi:10.1007/978-1-4757-4242-8_18. ISBN 978-1-4419-3461-1. PMID 15384578.
- ^ Senadhi, V (2011 Jul). "A paradigm shift in the outpatient approach to liver function tests". Southern Medical Journal. 104 (7): 521–5. doi:10.1097/SMJ.0b013e31821e8ff5. PMID 21886053.
{{cite journal}}: Check date values in:|date=(help) - ^ Halliday, John; Klenerman, Paul; Barnes, Eleanor (2011 May). "Vaccination for hepatitis C virus: closing in on an evasive target". Expert Review of Vaccines. 10 (5): 659–72. doi:10.1586/erv.11.55. PMC 3112461. PMID 21604986.
{{cite journal}}: Check date values in:|date=(help) - ^ Hagan, H.; Pouget, E. R.; Des Jarlais, D. C. (2011-07-01). "A systematic review and meta-analysis of interventions to prevent hepatitis C virus infection in people who inject drugs". The Journal of Infectious Diseases. 204 (1): 74–83. doi:10.1093/infdis/jir196. PMC 3105033. PMID 21628661.
- ^ Torresi, Joseph; Johnson, Doug; Wedemeyer, Heiner (2011 Jun). "Progress in the development of preventive and therapeutic vaccines for hepatitis C virus". Journal of Hepatology. 54 (6): 1273–85. doi:10.1016/j.jhep.2010.09.040. PMID 21236312.
{{cite journal}}: Check date values in:|date=(help) - ^ Ilyas, J. A.; Vierling, J. M. (2011 Aug). "An overview of emerging therapies for the treatment of chronic hepatitis C.". Clinics in Liver Disease. 15 (3): 515–36. doi:10.1016/j.cld.2011.05.002. PMID 21867934.
{{cite journal}}: Check date values in:|date=(help) - ^ Foote BS, Spooner LM, Belliveau PP (September 2011). "Boceprevir: a protease inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother. 45 (9): 1085–93. doi:10.1345/aph.1P744. PMID 21828346.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Smith LS, Nelson M, Naik S, Woten J (May 2011). "Telaprevir: an NS3/4A protease inhibitor for the treatment of chronic hepatitis C". Ann Pharmacother. 45 (5): 639–48. doi:10.1345/aph.1P430. PMID 21558488.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Ghany MG, Nelson DR, Strader DB, Thomas DL, Seeff LB (October 2011). "An update on treatment of genotype 1 chronic hepatitis C virus infection: 2011 practice guideline by the American Association for the Study of Liver Diseases". Hepatology. 54 (4): 1433–44. doi:10.1002/hep.24641. PMC 3229841. PMID 21898493.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Alavian SM, Tabatabaei SV (April 2010). "Treatment of chronic hepatitis C in polytransfused thalassaemic patients: a meta-analysis". J. Viral Hepat. 17 (4): 236–44. doi:10.1111/j.1365-2893.2009.01170.x. PMID 19638104.
{{cite journal}}: CS1 maint: date and year (link) - ^ a b Hepatitis C and CAM: What the Science Says. NCCAM March 2011. (Retrieved 07 March 2011)
- ^ Liu, J.; Manheimer, E.; Tsutani, K.; Gluud, C. (2003 Mar). "Medicinal herbs for hepatitis C virus infection: a Cochrane hepatobiliary systematic review of randomized trials". The American Journal of Gastroenterology. 98 (3): 538–44. doi:10.1111/j.1572-0241.2003.07298.x. PMID 12650784.
{{cite journal}}: Check date values in:|date=(help) - ^ Rambaldi, A.; Jacobs, B. P.; Gluud, C. (2007-10-17). "Milk thistle for alcoholic and/or hepatitis B or C virus liver diseases". Cochrane Database of Systematic Reviews (Online). 2007 (4): CD003620. doi:10.1002/14651858.CD003620.pub3. PMC 8724782. PMID 17943794.
- ^ Fung J, Lai CL, Hung I; et al. (September 2008). "Chronic hepatitis C virus genotype 6 infection: response to pegylated interferon and ribavirin". The Journal of Infectious Diseases. 198 (6): 808–12. doi:10.1086/591252. PMID 18657036.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ a b c "WHO Hepatitis C factsheet". 2011. Retrieved 2011-07-13.
- ^ Colacino, ed. by J. M. (2004). Hepatitis prevention and treatment. Basel: Birkhäuser. p. 32. ISBN 9783764359560.
{{cite book}}:|first=has generic name (help); Unknown parameter|coauthors=ignored (|author=suggested) (help) - ^ al.], edited by Gary W. Brunette ... [et (12 May 2011). CDC health information for international travel : the Yellow Book 2012. New York: Oxford University. p. 231. ISBN 9780199769018.
{{cite book}}:|first=has generic name (help) - ^ a b Boyer, JL (2001). Liver cirrhosis and its development: proceedings of the Falk Symposium 115. Springer. pp. 344. ISBN 9780792387602.
- ^ Choo QL, Kuo G, Weiner AJ, Overby LR, Bradley DW, Houghton M (April 1989). "Isolation of a cDNA clone derived from a blood-borne non-A, non-B viral hepatitis genome". Science. 244 (4902): 359–62. doi:10.1126/science.2523562. PMID 2523562.
{{cite journal}}: CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Kuo G, Choo QL, Alter HJ; et al. (April 1989). "An assay for circulating antibodies to a major etiologic virus of human non-A, non-B hepatitis". Science. 244 (4902): 362–4. doi:10.1126/science.2496467. PMID 2496467.
{{cite journal}}: Explicit use of et al. in:|author=(help)CS1 maint: date and year (link) CS1 maint: multiple names: authors list (link) - ^ Winners Albert Lasker Award for Clinical Medical Research, The Lasker Foundation. Retrieved 20 February 2008.
- ^ Houghton, M., Q.-L. Choo, and G. Kuo. NANBV Diagnostics and Vaccines. European Patent No. EP-0-3 18-216-A1. European Patent Office (filed 18 November 1988, published 31 May 1989).
- ^ Wilken, Judge. "United States Court of Appeals for the Federal Circuit". Retrieved 11 January 2012.
- ^ Eurosurveillance editorial, team (2011-07-28). "World Hepatitis Day 2011". Euro Surveillance : Bulletin Europeen Sur les Maladies Transmissibles = European Communicable Disease Bulletin. 16 (30). PMID 21813077.
- ^ a b Wong, JB (2006). "Hepatitis C: cost of illness and considerations for the economic evaluation of antiviral therapies". PharmacoEconomics. 24 (7): 661–72. doi:10.2165/00019053-200624070-00005. PMID 16802842.
- ^ a b El Khoury, A. C.; Klimack, W. K.; Wallace, C.; Razavi, H. (1 December 2011). "Economic burden of hepatitis C-associated diseases in the United States". Journal of Viral Hepatitis. 19 (3): 153–160. doi:10.1111/j.1365-2893.2011.01563.x. PMID 22329369.
- ^ "Hepatitis C Prevention, Support and Research ProgramHealth Canada". Public Health Agency of Canada. Nov 2003. Retrieved 10 January 2012.
{{cite web}}: CS1 maint: date and year (link) - ^ Zuckerman, edited by Howard Thomas, Stanley Lemon, Arie (2008). Viral Hepatitis (3rd ed.). Oxford: John Wiley & Sons. p. 532. ISBN 9781405143882.
{{cite book}}:|first=has generic name (help)CS1 maint: multiple names: authors list (link) - ^ Ahn, Joseph; Flamm, Steven L. (2011 Aug). "Hepatitis C therapy: other players in the game". Clinics in Liver Disease. 15 (3): 641–56. doi:10.1016/j.cld.2011.05.008. PMID 21867942.
{{cite journal}}: Check date values in:|date=(help) - ^ Vermehren, J.; Sarrazin, C. (2011 Feb). "New HCV therapies on the horizon". Clinical Microbiology and Infection : The Official Publication of the European Society of Clinical Microbiology and Infectious Diseases. 17 (2): 122–34. doi:10.1111/j.1469-0691.2010.03430.x. PMID 21087349.
{{cite journal}}: Check date values in:|date=(help)

